Memoria metabólica: El secreto epigenético de las enfermedades crónicas
Sep 22, 2025
¿Alguna vez te has preguntado por qué, después de haber perdido peso o de haber logrado un buen control de tu glucosa, tu cuerpo parece seguir arrastrando los problemas de antes? Es como si tus células "recordaran" los tiempos difíciles. Este fenómeno, intrigante y frustrante a la vez, se conoce como memoria metabólica.
Para entenderlo mejor, podemos recurrir al concepto de histéresis. En física, la histéresis describe la tendencia de un material a no responder de forma inmediata o lineal a un cambio en un campo externo, conservando una "memoria" de su estado anterior. Por ejemplo, un imán no pierde su magnetismo al instante al retirar el campo magnético. En biología, este concepto se aplica de manera similar: el cuerpo no vuelve a un estado de normalidad de inmediato después de que un estímulo dañino (como la hiperglucemia o la obesidad) desaparece. La histéresis metabólica explica que el organismo retiene un "eco" biológico del pasado, desafiando la idea de que una vez corregido el problema, todo vuelve a la normalidad de inmediato. Este es un concepto que surgió de ensayos clínicos de diabetes, que demostraron que un control glucémico temprano ofrecía beneficios duraderos que persistían incluso después de que los pacientes volvieran a un control peor (Tonna et al., 2010; Dong et al., 2024). Este concepto ha revolucionado la forma en que entendemos y tratamos las enfermedades crónicas, revelando que el problema no siempre está en el presente, sino en una persistencia biológica del pasado
¿Por qué sigo con problemas si ya me cuido?
La memoria metabólica se sustenta en tres pilares clave que explican su naturaleza y efectos duraderos:
-
Persistencia: Los efectos dañinos de un estado metabólico anormal, como la inflamación o el estrés oxidativo, no se desvanecen. Continúan o incluso se aceleran, aun después de que el entorno metabólico regresa a la normalidad.
-
Progresión o efecto progresivo: La duración y gravedad de las complicaciones a largo plazo dependen en gran medida del control metabólico temprano. Un buen control inicial puede mitigar el riesgo de complicaciones futuras, mientras que un control tardío tiene un impacto limitado en la progresión de daños ya establecidos.
-
Regulación epigenética: Este es el mecanismo molecular que establece y mantiene la persistencia. La epigenética no altera la secuencia de ADN, pero regula la expresión de los genes, traduciendo un estímulo ambiental (hiperglucemia u obesidad) en cambios a largo plazo en la función celular.
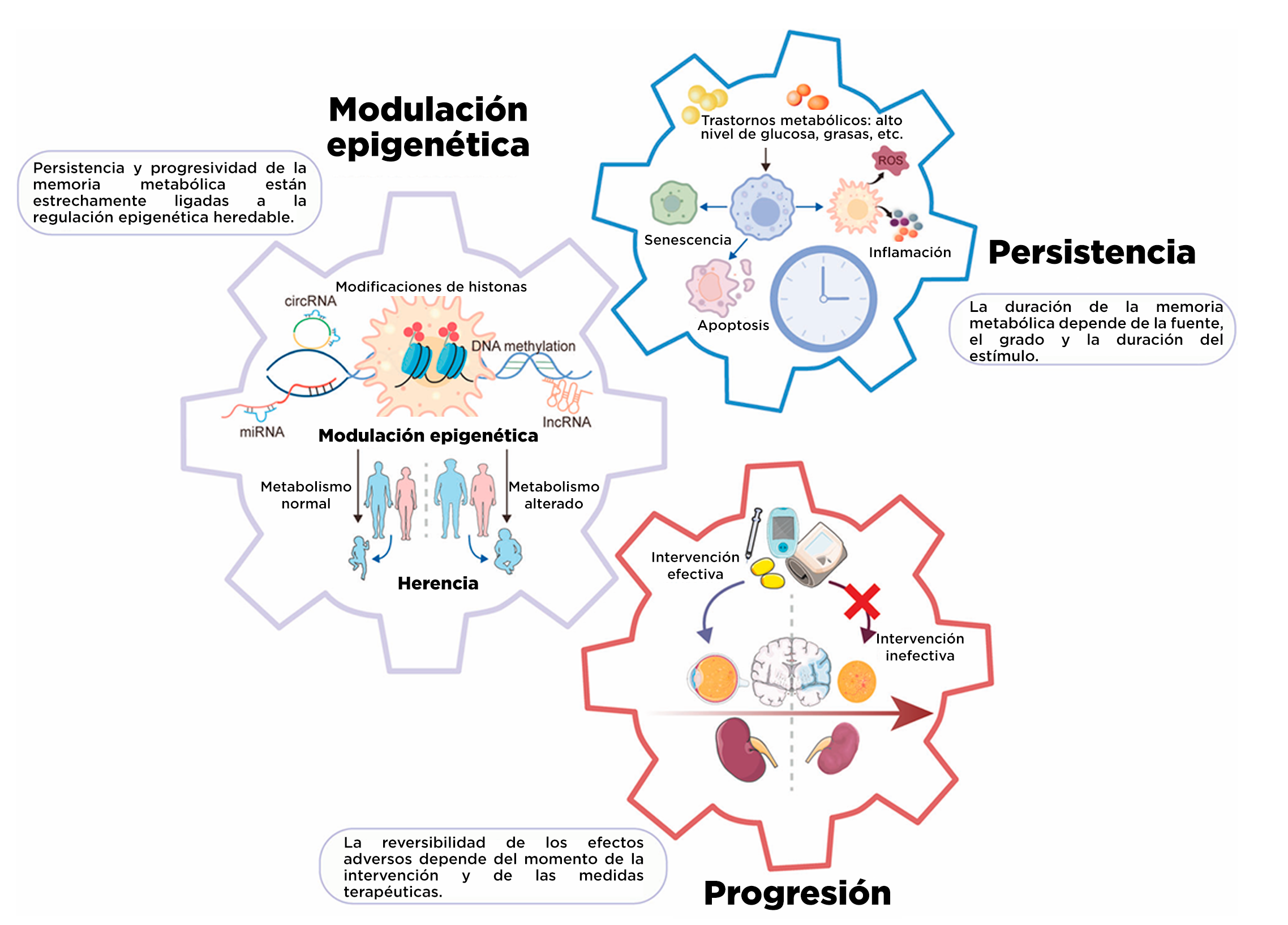
Imagen 1: Características de la memoria metabólica. La memoria metabólica presenta tres características distintivas. En primer lugar, los efectos adversos a largo plazo sobre las complicaciones diabéticas dependen del control glucémico temprano, ya que el control glucémico posterior no previene la progresión. En segundo lugar, la memoria metabólica promueve cambios inflamatorios, senescencia celular prematura y apoptosis continua, perpetuando los efectos nocivos incluso después de la resolución de la hiperglucemia. En tercer lugar, el establecimiento de la memoria metabólica está estrechamente asociado con modificaciones epigenéticas, lo que contribuye a la persistencia de los efectos adversos y a la progresión de las complicaciones diabéticas. Adaptada de Dong et al.
El secreto de este "eco o recuerdo" celular no está en nuestros genes, sino en la epigenética, una capa de información que controla la forma en que los genes se encienden o se apagan. La epigenética es como una serie de interruptores que le dicen a la célula qué genes debe usar y cuáles no. En la memoria metabólica, un estado de estrés (por exceso de glucosa o grasa) provoca cambios epigenéticos que se quedan "fijos" y continúan alterando el funcionamiento celular, incluso cuando el estímulo inicial ya no está.
Los mecanismos epigenéticos principales que perpetúan este fenómeno son:
-
Metilación del ADN: Imagina que es un grupo de candados que se colocan en los genes. Un ambiente metabólico alterado puede activar un tipo de "candado" que bloquea la expresión de genes protectores (como los que mantienen la salud de las mitocondrias) o que deja abiertos los genes que promueven la inflamación. Lo más asombroso es que estos candados persisten, transmitiendo la señal de daño a las nuevas células.
-
Modificaciones de histonas: Las histonas son proteínas alrededor de las cuales se enrolla el ADN. Piensa en ellas como el carrete de un hilo. El estado metabólico puede modificar estas histonas, haciendo que el ADN se enrolle de forma más o menos apretada. Si el ADN se enrolla mal, los genes de la inflamación o la fibrosis se mantienen accesibles y activos (Tonna et al., 2010).
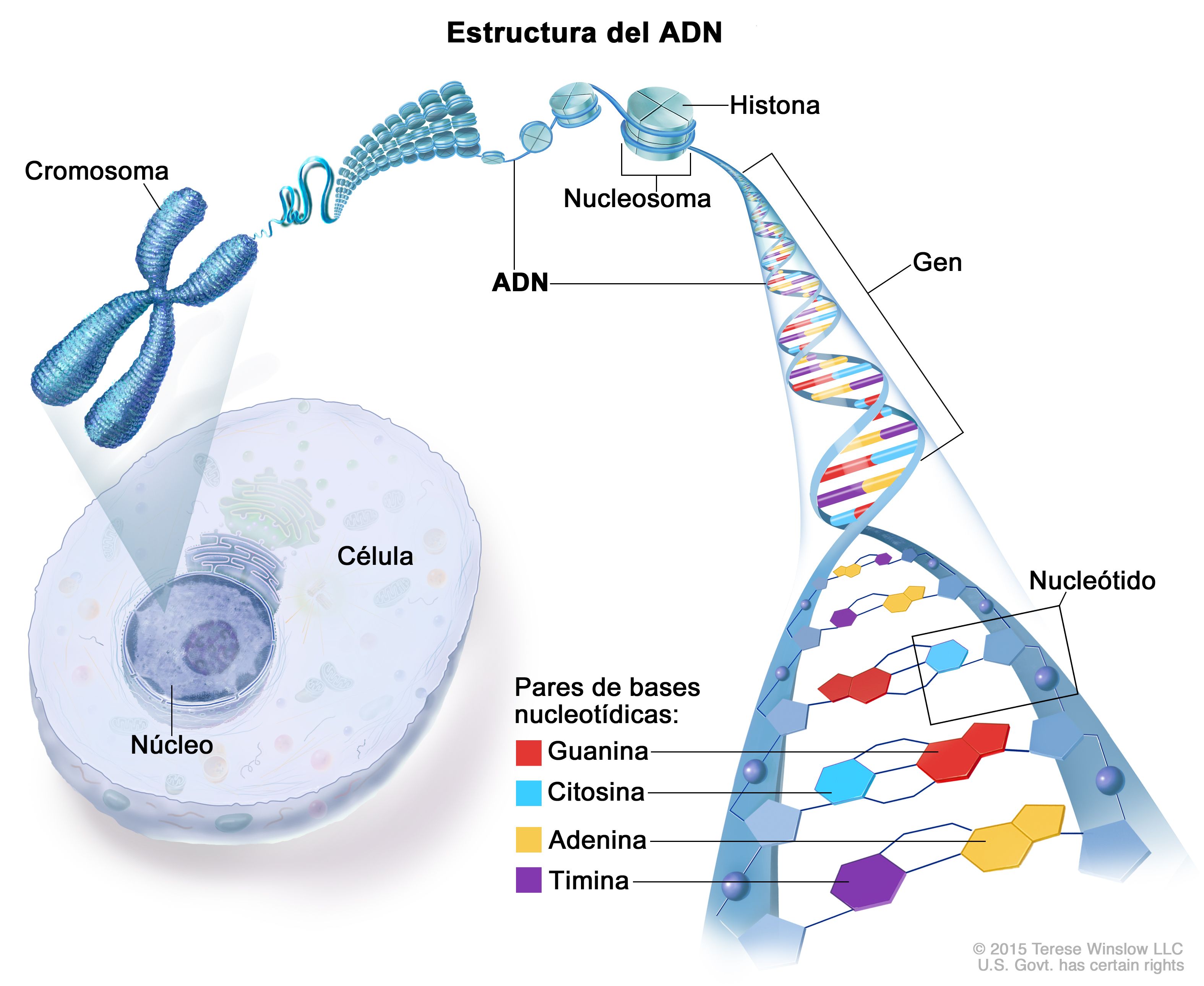
Imagen 2: Estructura del ADN. La mayor parte del ADN se encuentra en el interior del núcleo de una célula, donde forma los cromosomas. Los cromosomas contienen proteínas llamadas histonas que se unen al ADN. El ADN tiene dos cadenas que se enroscan y forman un espiral parecido a una escalera de caracol que se llama hélice. Los cuatro componentes básicos del ADN son los nucleótidos: adenina (A), timina (T), guanina (G) y citosina (C). Los nucleótidos se unen entre sí (A con T y G con C) mediante enlaces químicos y forman pares de bases que conectan las dos cadenas de ADN. Los genes son pequeñas piezas de ADN que tienen información genética específica.
-
ARN No Codificantes (ncRNAs): Estas moléculas de ARN no crean proteínas, pero son cruciales para regular la expresión génica. En la memoria metabólica, su desregulación puede amplificar las señales de daño, perpetuando vías patológicas como las que llevan a la fibrosis o la apoptosis celular (Dong et al., 2024).
Herencia epigenética transgeneracional: El impacto que tiene nuestro metabolismo en nuestros hijos
Investigaciones reciente han revelado una implicación aún más profunda de la memoria metabólica: su capacidad de ser transmitida a la siguiente generación. La persistencia y progresividad de la memoria metabólica están estrechamente ligadas a la regulación epigenética heredable. Esto significa que los cambios inducidos por un metabolismo desordenado en los padres (por ejemplo, a través de la obesidad o la hiperglucemia) pueden alterar el epigenoma de sus células reproductivas, lo que potencialmente puede predisponer a sus hijos a desarrollar enfermedades metabólicas o crónicas en el futuro. Este fenómeno, conocido como herencia epigenética transgeneracional, subraya la importancia del bienestar metabólico no solo para nuestra salud individual, sino también para la salud de las futuras generaciones.
Dos casos de estudio clave
-
El efecto rebote y el tejido adiposo: ¿Sabes por qué es tan difícil mantener el peso después de una dieta o una cirugía bariátrica? La investigación muestra que el tejido adiposo (la grasa) tiene una memoria obesogénica (memoria metabólica en los adipocitos, las células que almacenan grasa en nuestro cuerpo). Después de la pérdida de peso, las células de grasa conservan cambios epigenéticos que las predisponen a recuperar peso más rápidamente si se exponen de nuevo a una dieta alta en grasas (Hinte et al., 2024). Están "preparadas" para respuestas patológicas, volviendo a ganar peso de manera acelerada.
-
Complicaciones diabéticas: La memoria metabólica fue descubierta en pacientes con diabetes. A pesar de un control estricto de la glucosa, muchos continuaban desarrollando complicaciones como retinopatía y nefropatía (daños en la vista y los riñones) (Kato & Natarajan, 2019). Los científicos descubrieron que la hiperglucemia previa había causado un daño duradero a nivel celular y que las mitocondrias (las "fábricas de energía" de las células) se habían vuelto disfuncionales. Esta disfunción, impulsada por cambios epigenéticos, se mantuvo incluso después de normalizar el azúcar en sangre, explicando la progresión de estas enfermedades.
Acciones prácticas
Entender este concepto no es solo para los científicos; tiene un impacto directo en nuestra vida diaria. Aunque revertir la memoria metabólica es un gran desafío, la ciencia nos da algunas pistas sobre cómo mitigar su impacto:
-
Intervención temprana y sostenida: La evidencia clínica es clara: el mejor momento para controlar tu metabolismo es ahora. Cuanto antes se implementen hábitos de vida saludables para el control de la glucosa y el peso, más se reducirá la posibilidad de que se establezca un entorno metabólico dañino. No se trata solo de bajar de peso, sino de mantener los hábitos que te permiten sostener un metabolismo saludable.
-
Enfoque holístico en el bienestar: El cuidado no debe limitarse al peso, la glucosa o el perfil de lípidos. El estrés oxidativo (Dong et al., 2024) y la inflamación crónica son factores clave que perpetúan la memoria metabólica. Incorpora hábitos que los combatan, como una dieta antiinflamatoria, rica en antioxidantes (variedad de vegetales), ejercicio regular (no necesariamente gym, aumentar la cantidad de movimiento diario genera una mejoría sostenida) y un buen manejo del estrés (meditación, yoga, buen descanso).
- El ayuno profundo como herramienta metabólica: El ayuno a diferencia de lo que habitualmente se cree no es la dieta de moda, sino una herramienta metabólica poderosísima, ya que ayuda a equilibrar el entorno metabólico moderno (acceso infinito a calorías), con el "statu quo" de la vida (periodos de restricción calórica). El ayuno profundo es la única herramienta GRATUITA que tenemos a disposición para modificar el metabolismo desde adentro, el ayuno profundo bien ejecutado logra mejorar radicalmente la función celular, recuperando el equilibrio metabólico entre procesos anabólicos (crecimiento) y catabólicos (degradación). Te invitamos a nuestro 3er ayuno profundo en comunidad para generar un Reset profundo a tu cuerpo, da click aqui para ingresa a nuestra comunidad en whatsapp y conocer los detalles.

-
No te rindas: El concepto de memoria metabólica puede sonar desalentador, pero es un llamado a la acción. Si has tenido un pasado de malos hábitos, tu cuerpo necesitará un esfuerzo extra para sanar por completo. Nuestra mejor recomendación será buscar un grupo de personas que te inspiren, enseñen y que vivan el bienestar, ya que gozar de buena salud requiere tanto de acciones sostenibles como de un cambio de identidad. Sé paciente y consistente. El objetivo no es solo alcanzar una cifra en la báscula, sino restaurar el correcto funcionamiento de tus células a largo plazo.
Conclusión
La memoria metabólica nos enseña que el bienestar no es un estado fijo, sino un proceso dinámico y persistente. Nuestro pasado metabólico puede influir en nuestro futuro, pero esto no significa que estemos condenados. Al entender los mecanismos detrás de esta memoria, podemos ser más conscientes de la importancia de la prevención y de mantener un estilo de vida saludable de forma consistente a lo largo del tiempo. La verdadera salud no está en las dietas de moda o las soluciones rápidas, sino en el compromiso diario de cuidar nuestro cuerpo a nivel más profundo, hasta un nivel celular.
Con aprecio, Leo Arévalo ❤
Fundador OUTLIERS
Referencias
- Hinte, L. C., Castellano-Castillo, D., Ghosh, A., Melrose, K., Gasser, E., Noé, F., Massier, L., Dong, H., Sun, W., Hoffmann, A., Wolfrum, C., Rydén, M., Mejhert, N., Blüher, M., & Von Meyenn, F. (2024). Adipose tissue retains an epigenetic memory of obesity after weight loss. Nature. https://doi.org/10.1038/s41586-024-08165-7
-
Kowluru, R. A., & Mohammad, G. (2020). Epigenetics and Mitochondrial Stability in the Metabolic Memory Phenomenon Associated with Continued Progression of Diabetic Retinopathy. Scientific Reports, 10(1). https://doi.org/10.1038/s41598-020-63527-1
-
Kato, M., & Natarajan, R. (2019). Epigenetics and epigenomics in diabetic kidney disease and metabolic memory. Nature Reviews Nephrology, 15(6), 327–345. https://doi.org/10.1038/s41581-019-0135-6
-
Dempsey, L. A. (2012). Memory metabolism. Nature Immunology, 13(3), 213. https://doi.org/10.1038/ni.2253
-
Tonna, S., El-Osta, A., Cooper, M. E., & Tikellis, C. (2010). Metabolic memory and diabetic nephropathy: potential role for epigenetic mechanisms. Nature Reviews Nephrology, 6(6), 332–341. https://doi.org/10.1038/nrneph.2010.55
-
Dong, H., Sun, Y., Nie, L., Cui, A., Zhao, P., Leung, W. K., & Wang, Q. (2024). Metabolic memory: mechanisms and diseases. Signal Transduction and Targeted Therapy, 9(1). https://doi.org/10.1038/s41392-024-01755-x
La información presentada en esta obra es simple material informativo y no pretende servir de diagnóstico, prescripción o tratamiento de cualquier tipo de dolencia. Esta información no sustituye la consulta con un médico, especialista o cualquier otro profesional competente del campo de la salud. El contenido de la obra debe considerarse un complemento a cualquier programa o tratamiento prescrito por un profesional competente de la medicina. Los autores están exentos de toda responsabilidad sobre daños y perjuicios, pérdidas o riesgos, personales o de cualquier otra índole, que pudieran producirse por el mal uso de la información aquí proporcionada. Reservados todos los derechos. Para más información visita www.outliers.university





